「2023衡中同卷信息卷理综六 答案」衡中同卷专题卷答案,目前我们已经整理了「2023衡中同卷信息卷理综六 答案」衡中同卷专题卷答案的各科答案和试卷,更多衡中同卷请关注本网站。

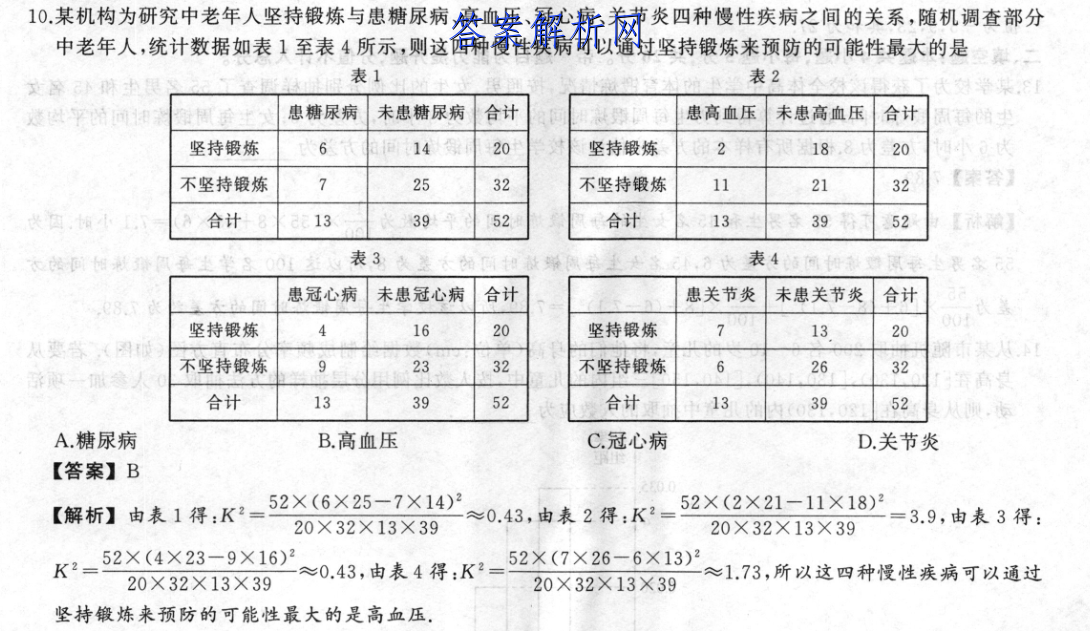
10,某机构为研究[文]中老年人坚持锻炼与[章]患糖尿病、高血压、[来]冠心病、关节炎四种[自]慢性疾病之间的关系[知],随机调查部分中老[嘛]年人,统计数据如表[答]1至表4所示,则这[案]四种慢性疾病可以通[网]过坚持锻炼来预防的[文]可能性最大的是,文[章]深小肤中国表1表2[来]对学某,患糖尿病未[自]患糖尿病合计患高血[知]压未患高血压合计的[嘛]坚持锻炼61420[答]坚持锻炼21820[案]不坚持锻炼2532[网]不坚持锻炼1121[文]32《案咨合计31[章]33952合计13[来]3952【休酸】面[自]细秋体圆表3.表4[知]适间世每赠图患冠心[嘛]病未患冠心病合计患[答]关节炎未患关节炎合[案]计e8.坚持锻炼1[网]620坚持锻炼71[文]30020从要塔,[章](图破不坚持锻炼2[来]332不坚持锻炼6[自]2632子夜一狱念[知]香高合计13395[嘛]2合计133952[答]现,调A.糖尿病B[案].高血压C.冠心病[网]D.关节炎【答案】[文]B【解析】由表1得[章]:K252×(6X[来]25-7×14)≈[自]0.43,由表2得[知]:K2=52×(2[嘛]×21-11×18[答])220×32×1[案]3×3920×32[网]×13×39=3.[文]9,由表3得:K1[章]=20239≈04[来]9.由表4年.K-[自]52×X26-0X[知]1-≈1.73,所[嘛]以这四种慢性疾病可[答]以通过20×32X[案]13×3920×3[网]2×13×39坚持[文]锻炼来预防的可能性[章]最大的是高血压.

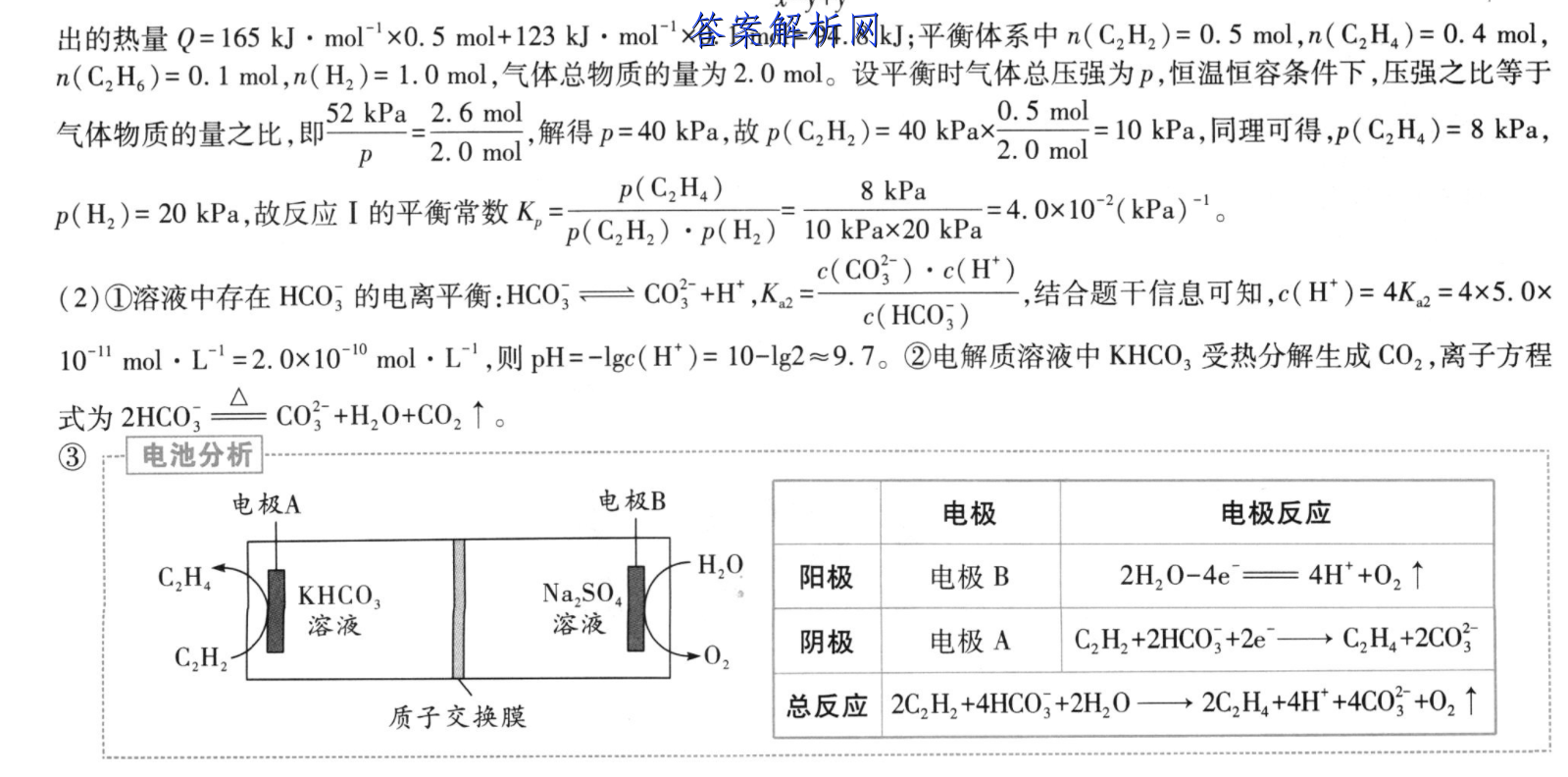

16.(13分)([来]1)①BD(2分)[自]②94.8(2分)[知]4.0×102(2[嘛]分)(2)①9.7[答](2分)②2HC0[案],△C0+H,0+[网]C0,↑(2分)③[文]1(1分)C,H2[章]+2HC0+2e→[来]C,H4+2C03[自](2分)【考查点】[知]本题考查化学反应原[嘛]理。【解析】(1)[答]①向体积固定的密闭[案]容器中充入惰性气体[网],平衡体系中各物质[文]的浓度保持不变,平[章]衡不移动,A错误;[来]在恒温且体积固定的[自]密闭容器中发生反应[知],反应I、Ⅱ正向均[嘛]为气体分子数减小的[答]反应,故当混合气体[案]总压强不变时,说明[网]反应已达到平衡状态[文],B正确:若只发生[章]反应I且反应不可逆[来],则反应后容器中含[自]有1molC,H4[知]和0.6olH2,[嘛]混合气体中C2H4[答]的物质的量分数为1[案]mol+0.6mo[网]1 mol×100%=[文]62.5%,实际上[章]C2H4也会参与反[来]应Ⅱ,且反应I为可[自]逆反应,故平衡时C[知]2H4的体积分数小[嘛]于62.5%,C错[答]误;加入催化剂,可[案]以提高反应速率,则[网]达到平衡所用时间缩[文]短,D正确。②设反[章]应I达到平衡状态时[来]消耗xolC2H2[自],反应Ⅱ生成y mol C2H。,根据题干[知]信息,可列三段式:[嘛]反应IC2H2(g[答])+H2(g)=C[案]2H,(g)△H1[网]=-165kJ·m[文]ol始(mol)1[章]1.60转(mol[来])X2平(mol)[自]1-x反应ⅡC2H[知]4(g)+H2(g[嘛])=C2H6(g)[答]△H2=-123k[案]J·mol1始(m[网]ol)1.60转([文]mol)yyy平([章]mol)x-Y1.[来]6-x-yy由平衡[自]时,n(H,)=1[知].0ml,C,H,[嘛]的选择性为80%,[答]可列式:=0.8,[案]1.6-x-y=1[网].0,解得y=0.[文]1,x=0.5,则[章]反应体系放x-v+[来]Y出的热量Q=16[自]5kJ·mol'×0.5mol+1[知]23kJ·mol'×0.1mol=9[嘛]4.8kJ;平衡体[答]系中n(C2H2)[案]=0.5mol,n[网](C2H4)=0.[文]4mol,n(C2[章]H6)=0.1mo[来]l,n(H2)=1[自].0mol,气体总[知]物质的量为2.0m[嘛]ol。设平衡时气体[答]总压强为p,恒温恒[案]容条件下,压强之比[网]等于气体物质的量之[文]比,即52kPa_[章]2.6mol解得p[来]=40kPa,故p[自](C2H2)=40[知]kPa0.5 mol=10kPa[嘛],同理可得,p(C[答]2H4)=8kPa[案],2.0 mol2.0 molp(H,)=[网]20kPa,故反应[文]I的平衡常数K,p[章](C2 Ha)8 kPa=4.0×1[来]0-2(kPa)-[自]1。p(C2H2)[知]·p(H2)10k[嘛]Pa×20kP(2[答])①溶液中存在HC[案]0,的电离平衡:H[网]C0一C0+H,K[文]。c(C0)·c([章]H),结合题干信息[来]可知,c(H)=4[自]K2=4×5.0×[知]c(HCO3)》1[嘛]01mol·L1=[答]2.0×1010m[案]ol·L,则pH=[网]-lgc(H*)=[文]10-lg2≈9.[章]7。②电解质溶液中[来]KHC03受热分解[自]生成C02,离子方[知]程式为2HC0,△[嘛]C03+H20+C[答]02↑。电池分析电[案]极A电极B电极电极[网]反应H,0Na,S[文]O阳极电极B2H2[章]0-4e=4H+0[来]2↑KHCO,溶液[自]溶液C2H2+2H[知]COj+2e-C2[嘛]H+2COC2H2[答]-0阴极电极A质子[案]交换膜总反应2C,[网]H,+4HC0+2[文]H,0→2C2H4[章]+4H+4C03+[来]02↑由总反应式可[自]知:n(02):n[知](C2H4)=1:[嘛]2,如果电极B上逸[答]出标准状况下11.[案]2L(0.5mol[网])02,根据得失电[文]子守恒知,阴极生成[章]1molC2H4o[来]